El desenvolupament de fàrmacs és d'alt risc i llarg. L'espera de possibles nous tractaments és difícil per als pacients, especialment aquells amb condicions rares o difícils de tractar, i si el mercat és petit, el cost del medicament aprovat pot ser elevat. Reutilitzar i reposicionar els fàrmacs existents (també conegut com a reprofiling) pot accelerar el procés i reduir la inversió financera necessària en comparació amb els nous fàrmacs, garantint que els pacients puguin accedir als tractaments més ràpidament i a uns costos més assequibles.[1, 2]
Hi ha quatre grups clau de fàrmacs reutilitzats: fàrmacs comercialitzats amb patents existents o caducades, fàrmacs que s'han acabat en etapes clíniques o reguladores, estereoisòmers o metabòlits de fàrmacs existents o candidats on s'han fet canvis menors als fàrmacs existents. És important recordar que el fracàs dels fàrmacs en els assaigs clínics no és només causat per problemes d'eficàcia o seguretat: pot ser perquè una empresa canvia de direcció, problemes amb la formulació o perquè hi ha hagut problemes d'interès comercial o una planificació estratègica deficient.[3]
Els beneficis de reutilitzar i reposicionar els medicaments
Tot i que els dos termes s'utilitzen sovint de manera intercanviable, la reutilització del medicament pot referir-se a prendre un medicament aprovat i utilitzar-lo per a una altra indicació. El reposicionament del fàrmac pot referir-se a reiniciar el desenvolupament d'un fàrmac que s'ha estancat, per obtenir l'aprovació d'una nova indicació.[1]
Els principals avantatges de reutilitzar o reposicionar els fàrmacs són l'aspecte de cost i temps. El període de temps per desenvolupar un fàrmac reutilitzat sol ser d'un a tres anys, en comparació amb una mitjana de 12 anys per a un fàrmac nou.[4]
Per a una empresa que desenvolupa un fàrmac que s'ha aturat en desenvolupament, o un que ha arribat al mercat per a una altra indicació, la capacitat de "reciclar" les dades de seguretat, toxicitat i farmacocinètica/farmacodinàmica preclíniques i/o clíniques existents estalviarà temps i diners. . També els permet recuperar els diners invertits en el que, d'altra manera, podria ser un fàrmac fallit. El coneixement existent també redueix el risc de fracàs.
Els fàrmacs que han fracassat o que estan fracassant en el desenvolupament, però encara tenen una certa protecció de patent, poden ser reposicionats per una altra indicació per part de l'empresa originadora o un llicenciatari. La reutilització també pot permetre a les empreses allargar el cicle de vida dels seus propis medicaments comercialitzats que s'acosten a la caducitat de la patent, ja que poden obtenir protecció per a la nova indicació. La reutilització i el reposicionament de fàrmacs també poden ser valuosos per a les empreses que desenvolupen fàrmacs per a malalties rares, fomentant la col·laboració i l'intercanvi de dades i recursos.[3, 5]
Els passos per desenvolupar i obtenir l'aprovació d'un medicament reutilitzat poden incloure:
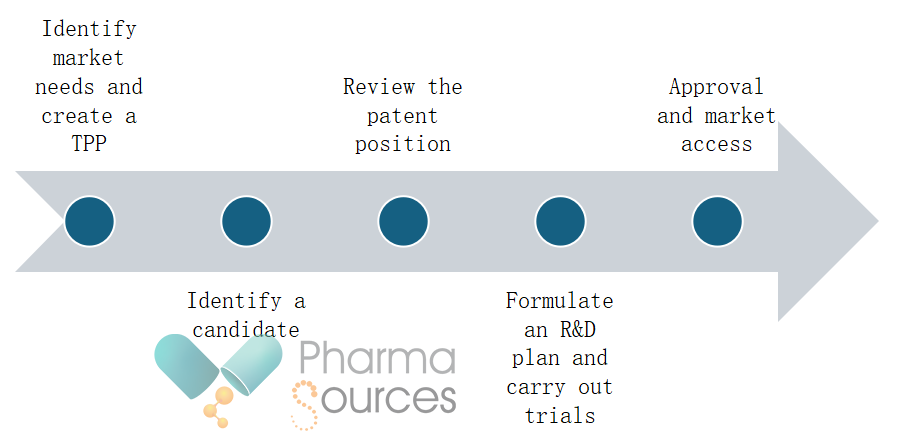
Identificar les necessitats del mercat i crear un perfil de producte objectiu
Per a una empresa que vol reutilitzar un medicament però no té un candidat existent en ment, el primer pas és avaluar el panorama del mercat per veure si hi ha una necessitat del pacient per un nou medicament i si l'empresa podrà recuperar-se. la inversió en el desenvolupament de fàrmacs. Això es recolza en el desenvolupament d'un perfil de producte objectiu (TPP). El TPP descriu les característiques desitjades d'un fàrmac en desenvolupament per a un trastorn específic. Proporciona a l'empresa una guia durant el desenvolupament de fàrmacs per a tots els equips implicats. [2, 6, 7]
Les àrees cobertes en un TPP, que també són útils per revisar quan una empresa té en ment un candidat específic, inclouen:[2, 7, 8]
●Indicació
○Indicació inicial de l'objectiu
○Possibles indicacions de futur
●Població
○Mercat objectiu inicial: prioritats econòmiques o àrees de major necessitat no satisfeta
○Estudi de viabilitat
○Requisit d'un diagnòstic complementari per identificar subpoblacions
●Orientació/farmacocinètica
●Seguretat, tolerabilitat i eficàcia
○Estudi els punts finals
○Beneficis en comparació amb competidors actuals/futurs o estàndard d'atenció
●Interaccions fàrmac-droga
●Estabilitat
○Requisits d'emmagatzematge
○Pot dependre dels mercats objectiu
●Via d'administració/formulació
○Formulació actual/potencial de reformulació
○Quina via d'administració serà la preferida pels pacients?
○Es requerirà un dispositiu de lliurament i ja està disponible?
●Freqüència de dosificació
○Tenir en compte en comparació amb l'estàndard d'atenció
●Cost
○Cost objectiu per dosi, basat en l'anàlisi del paisatge competitiu
●Temps de disponibilitat
○Temps necessari per a assajos clínics i processos reguladors
○Temps necessari per a les avaluacions de tecnologies sanitàries (HTA)
Identificar un candidat
Una empresa pot tenir en ment un medicament com a candidat a la reutilització, per exemple basant una nova indicació en una troballa vista com un efecte secundari en un procés de desenvolupament previ.

Per a una empresa que busca un medicament per a un objectiu o una indicació específica, els enfocaments poden estar basats en objectius, estructura, signatura, via, xarxa, coneixement o dades clíniques, amb enfocaments específics que inclouen:[13-17]
● Aleatorització mendeliana per establir relacions entre fenotips i efectes de fàrmacs predits genèticament
● Dades multiòmiques a gran escala per entendre millor l'etiologia de la malaltia i identificar noves dianes de fàrmacs
● Aprenentatge automàtic per identificar subtipus de malalties i dianes de fàrmacs, o per enllaçar patologia i mecanismes moleculars
● IA generativa o integració de l'expressió gènica humana, pertorbació de fàrmacs i dades clíniques, per identificar candidats
Revisar la posició de la patent
Una empresa que vulgui reutilitzar o reposicionar un medicament ha de conèixer la posició de patent existent, incloses les patents del compost original i les formulacions, els règims de dosificació o els usos específics. Si el medicament encara està cobert per una patent, hauran de posar-se en contacte amb el titular de la patent i veure si estan interessats a col·laborar o a llicenciar el medicament. Si el fàrmac no està patentat, hi ha més llibertat per operar.[4]
Tots els fàrmacs, inclosos els medicaments reutilitzats i reposicionats, necessiten un nivell de protecció de patents per permetre a l'empresa reutilitzadora recuperar els seus costos abans d'enfrontar-se a la competència. Els nous tipus de patents podrien incloure: [4, 18]
●Indicació terapèutica
●Formulació
●Règim de dosis
● Sistema de lliurament
● Combinació de fàrmacs
● Combinació fàrmac/dispositiu
Formular un pla d'R+D i realitzar assajos
Per desenvolupar amb èxit un fàrmac reutilitzat, les empreses han de treballar amb metges i un equip multidisciplinari d'experts interns i externs per donar suport al procés de desenvolupament. Els fàrmacs reutilitzats encara han de tenir dades preclíniques suficients, passar per assaigs clínics i complir els estàndards reglamentaris exigents en la seva nova indicació. Tot i que les dades humanes i no humanes existents donaran suport a la seguretat i la toxicitat, es necessitaran més estudis clínics per confirmar l'eficàcia en el grup de pacients objectiu abans de presentar-les per a l'aprovació.[8]També és important treballar amb pacients i grups de defensa de pacients, per entendre què necessiten d'un tractament i per reclutar participants per a assaigs clínics.[4]
Aprovació i accés al mercat
Una col·laboració estreta amb les autoritats reguladores i els organismes d'avaluació de tecnologies sanitàries (HTA) donarà suport a un procés eficient cap a l'aprovació, el mercat i el reemborsament. Les autoritats reguladores poden aconsellar quins assajos clínics seran necessaris i suggerir quina via d'aprovació, incloses les rutes accelerades, serà la més adequada per a un medicament i una indicació específics.[4]
En resum
La reutilització i el reposicionament de fàrmacs ofereix una ruta rendible i eficient al mercat que permet als pacients accedir als fàrmacs més ràpidament. Les empreses han d'assegurar-se que recullen les dades adequades per a un procés fluid, i això es pot ajudar col·laborant amb pacients, altres empreses, autoritats reguladores i organismes d'avaluació de tecnologies sanitàries.
Referències
1. Bakker, A., Un problema semàntic aparentment petit és un obstacle important per desenvolupar tractaments per a malalties rares. STAT, 2023. Disponible a: https://www.statnews.com/2023/06/27/drug-repurposing-repositioning-rare-diseases/.
2. Griffiths, A., et al., Target Product Profiles in Pharmaceutical Development KPMG. 2023. Disponible a: https://assets.kpmg.com/content/dam/kpmg/uk/pdf/2023/01/target-product-profiles-in-pharmaceutical-development.pdf.
3. Elvidge, S., Fer fora de l'ampolla el geni del reposicionament de drogues. Life Science Leader, 2010. Disponible a: https://www.lifescienceleader.com/doc/getting-the-drug-repositioning-genie-out-of-the-bottle-0001.
4. Pisani, J., et al., Repurposing medicines: the occasion and the challenge. 2021. Disponible a: https://www.lifearc.org/wp-content/uploads/2024/03/RD-Drug-repurposing-report.pdf.
5. Taylor, M., M. Salova i A. Schroeder, Reutilització de fàrmacs: potencial per expandir el tractament de malalties rares. Avalere: Insights & Analysis, 19 de febrer de 2024. Disponible a: https://avalere.com/insights/drug-repurposing-potential-to-expand-rare-disease-treatment.
6. Escriptor del personal. Perfils de productes objectiu. Organització Mundial de la Salut. 9 de juliol de 2024. Disponible a: https://www.who.int/observatories/global-observatory-on-health-research-and-development/analyses-and-syntheses/target-product-profile/who-target-product - perfils.
7. Escriptor del personal. Reutilització d'un fàrmac: consideracions clau. Xarxes d'innovació terapèutica de la UCL - UCL – University College London. 9 de juliol de 2024. Disponible a: https://www.ucl.ac.uk/ion/translation-enterprise/tailored-support-translational-researchers/re-purposing-drug/repurposing-drug.
8. Escriptor del personal. Guia per navegar pel procés. LifeArc/Consell d'Investigació Mèdica. 11 de juliol de 2024. Disponible a: https://www.repurposingmedicines.org.uk.
9. Taula rodona sobre la traducció de la investigació basada en la genòmica per a la salut, el Consell de Política de Ciències de la Salut i l'Institut de Medicina, a Drug Repurposing and Repositioning: Workshop Summary. 2014: Washington (DC).
10. Ghofrani, HA, IH Osterloh i F. Grimminger, Sildenafil: de l'angina a la disfunció erèctil a la hipertensió pulmonar i més enllà. Nat Rev Drug Discov, 2006. 5(8): pàg. 689-702.
11. Gohel, D., et al., Sildenafil com a medicament candidat per a la malaltia d'Alzheimer: observació de dades de pacients del món real i observacions mecàniques a partir de neurones derivades de cèl·lules mare pluripotents induïdes pel pacient. J Alzheimers Dis, 2024. 98(2): p. 643-657.
12. Grup Assessor de Medicaments de Dorset, GUIA D'ATENCIÓ COMPARTIDA DEL SILDENAFIL PER A LA GESTIÓ DEL FENÒMEN RAYNAUDS SECUNDARI ASSOCIAT A L'ESCLEROSI SISTÉMICA NHA. 2017. Disponible a: https://nhsdorset.nhs.uk/Downloads/aboutus/medicines-management/Shared%20Care%20Guidelines/Sildenafil%20Shared%20Care%20Documented%20July%2017.pdf.
13. Wang, L., et al., El paisatge de la metodologia en la reutilització de fàrmacs utilitzant dades genòmiques humanes: una revisió sistemàtica. Breu Bioinform, 2024. 25(2).
14. Sperry, M. i DE Ingber, Drug Repurposing Strategies, Challenges and Successes. 4 de març de 2024. Disponible a: https://www.technologynetworks.com/drug-discovery/articles/drug-repurposing-strategies-challenges-and-successes-384263#D3.
15. Rodríguez, S., et al., L'aprenentatge automàtic identifica candidats per a la reutilització de fàrmacs en la malaltia d'Alzheimer. Nat Commun, 2021. 12(1): p. 1033.
16. Yan, C., et al., Aprofitant la IA generativa per prioritzar els candidats a la reutilització de fàrmacs per a la malaltia d'Alzheimer amb validació clínica del món real. NPJ Digit Med, 2024. 7(1): pàg. 46.
17. Wu, P., et al., Integrant l'expressió gènica i les dades clíniques per identificar candidats a la reutilització de fàrmacs per a la hiperlipèmia i la hipertensió. Nat Commun, 2022. 13(1): p. 46.
18. Conour, J., Per què val la pena invertir el mètode de tractament de les patents per a medicaments reutilitzats. JD Supra: News & Insights, 5 d'octubre de 2020. Disponible a: https://www.jdsupra.com/legalnews/why-method-of-treatment-patents-for-92813/.

